2025-12-10
背景简介
在医药创新的征途中,Ken Song创立的RayzeBio以卓越的战略眼光和高效的执行力,书写了一段令人瞩目的传奇。短短三年间,RayzeBio凭借其在α核素(Ac-225)领域的前瞻性布局,以及对差异化靶点的精准选择,成功构建了极具竞争力的产品管线,并以惊人的速度推进临床开发,最终以41亿美元的高价被BMS收购,这一成就充分彰显了其在精准医疗领域的非凡实力。而最新收购Philochem的OncoACP3项目,靶向前列腺癌新兴靶点ACP3,不仅进一步丰富了RayzeBio的产品矩阵,更凸显了其在战略布局上的连贯性和前瞻性,为未来的持续发展奠定了坚实基础。本篇将重点聚焦于RayzeBio的两大核心产品管线——GPC3和ACP3,揭示其在靶点选择和市场布局上的独特优势。
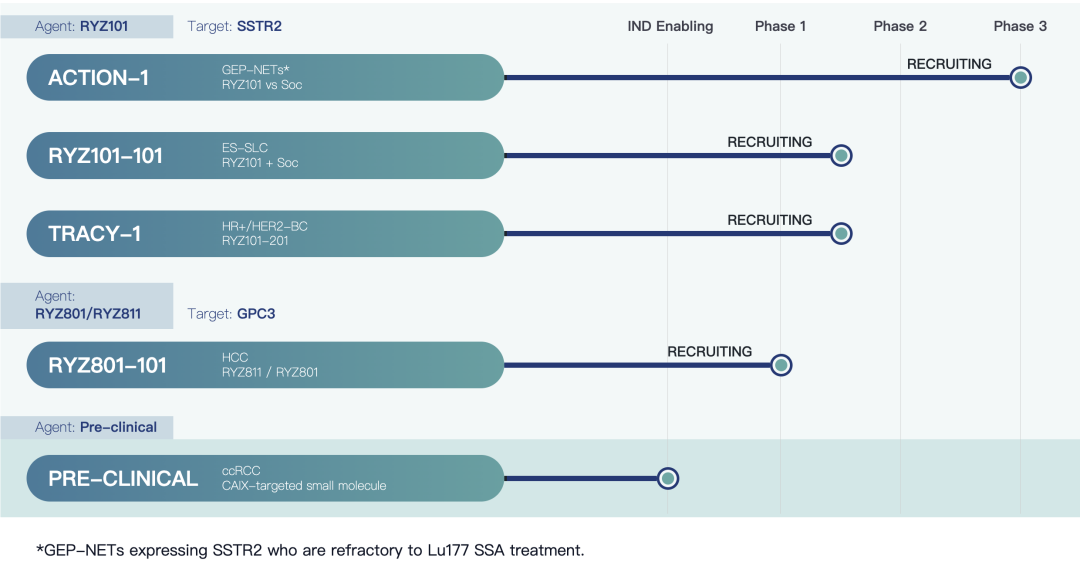
避开内卷,押注FIC靶点GPC3
目前全球范围内尚未有GPC3靶向药物获批上市。在肝癌治疗领域,RayzeBio采取差异化竞争策略,独辟蹊径地选择了Glypican-3(GPC3)这一极具潜力的创新靶点。GPC3作为肝癌特异性生物标志物,在超过70%的肝细胞癌中呈现高表达,而在正常组织中几乎不表达,这种独特的表达谱使其成为理想的治疗靶点。
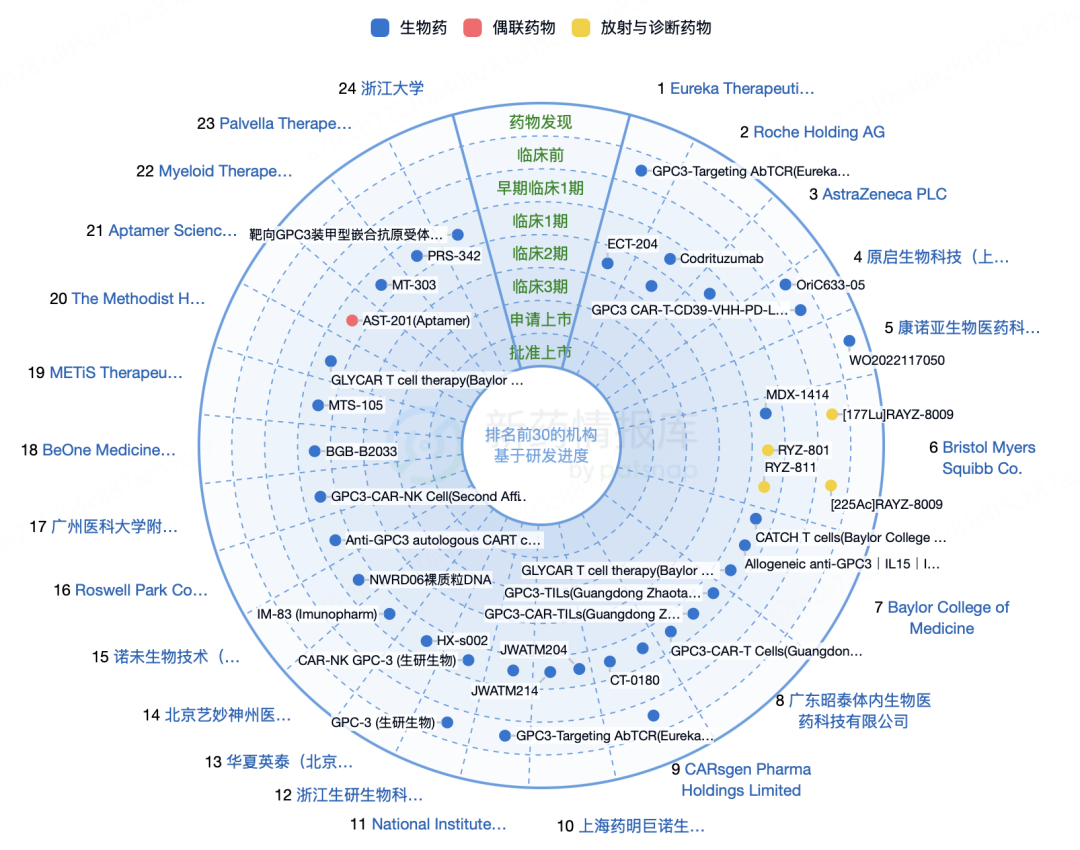
GPC靶点的药物研发状态(数据更新截至时间为2025.06.12)
RayzeBio通过与PeptiDream的战略合作,成功开发了全球首创的GPC3靶向放射性核素诊疗一体化平台。该平台创新性地整合了68Ga标记的PET显影剂(用于精准诊断)和177Lu/225Ac标记的治疗药物(用于靶向放射治疗),构建了"诊疗一体化"的完整解决方案。这一战略布局不仅填补了肝癌核素治疗领域的重大空白,更通过差异化创新在竞争激烈的肝癌治疗市场中开辟了新的赛道。
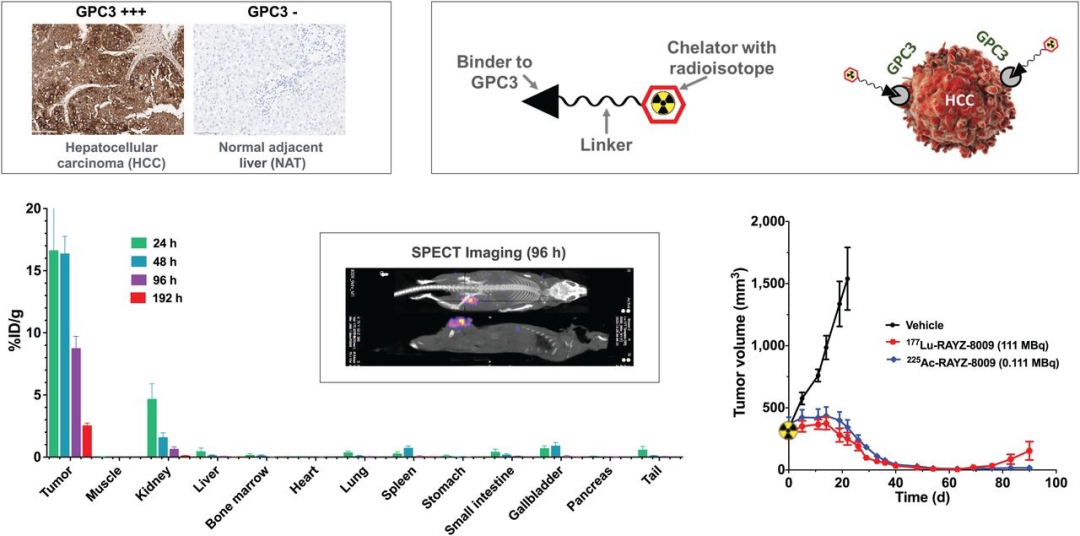
Journal of Nuclear Medicine February 2024, jnumed.123.266766
2024年,相关研究结果数据开始释放。据公开资料显示DOTA-RYZ-GPC3 (RAYZ-8009)由PeptiDream开发的环肽、连接子和螯合剂三部分组成,可与不同的放射性同位素结合,达到诊疗一体化的目的。临床前研究结果显示RAYZ-8009与人、小鼠、犬和食蟹猴的GPC3蛋白具有较高的结合亲和力,与其他Glypican家族成员无结合。在GPC3阳性的HepG2细胞中证实了有效的细胞结合与有效的内化,该结合并不受同位素更换的影响。177Lu-RAYZ-8009的生物分布研究表明,肿瘤显示出持续摄取和代谢器官肾脏的快清除,其他正常组织几乎没有摄取。原位肝细胞癌组织也表现出肿瘤特异性摄取,而健康肝组织未见摄取。在GPC3阳性HCC荷瘤模型中,177Lu-和225Ac标记的RAYZ-8009单药治疗和与lenvatinib联合治疗均获得了显著且持久的肿瘤消退和生存获益。
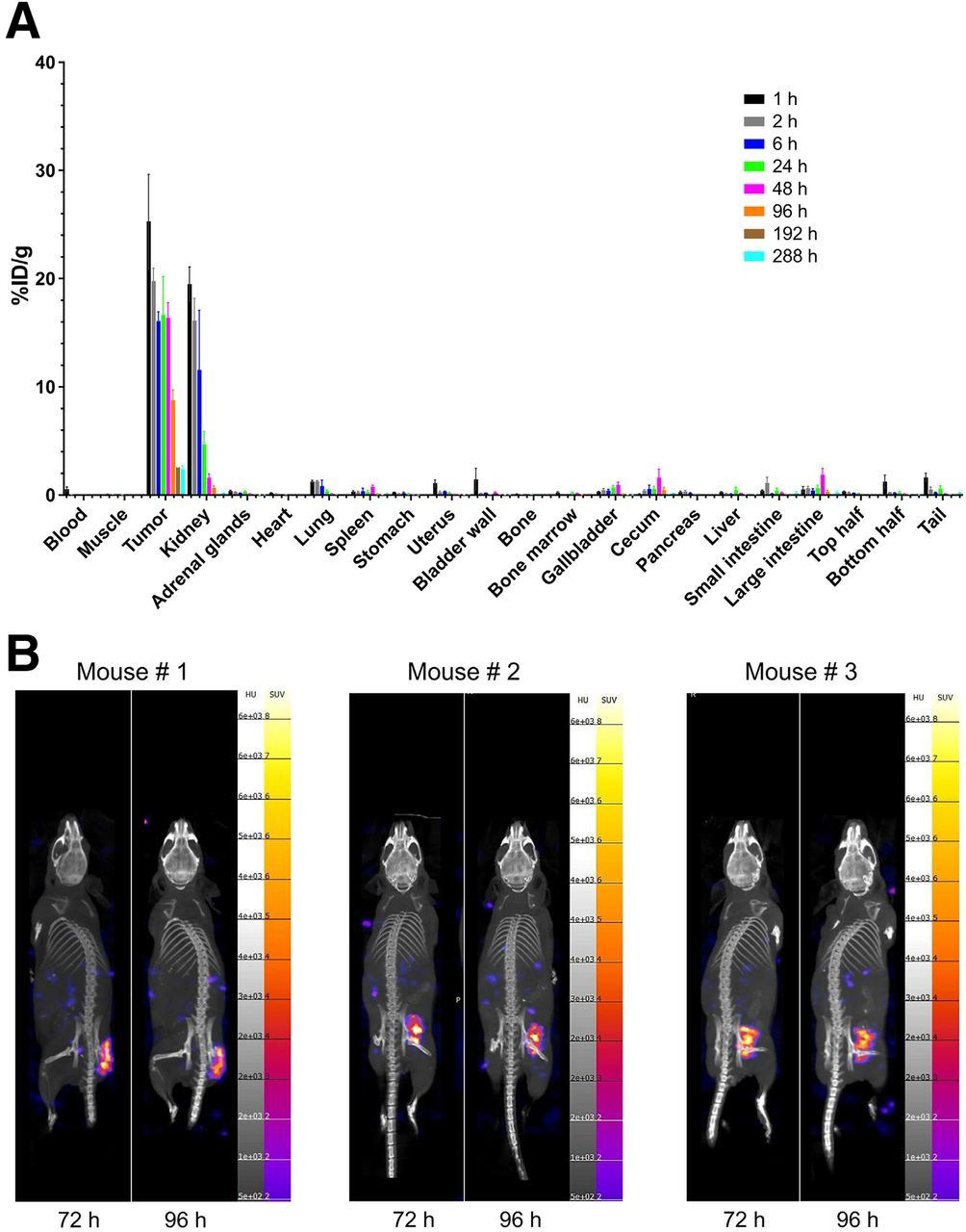
177Lu-RAYZ-8009在HepG2肿瘤小鼠中的生物分布和SPECT成像数据质量较高,基于HepG2体外生物分布数据的初步人类剂量测定估计表明,肾脏是剂量限制器官(0.0858 Gy/GBq,而肿瘤为0.779 Gy/GBq)。177Lu-RAYZ-8009在有肿瘤模型中表现出持续的肿瘤特异性摄取和快速的肾脏清除,持续的肿瘤滞留可能是与GPC3的高结合亲和力和有效内化的结果。HepG2肿瘤信号在不同时间点都一直高于肾脏的信号,肿瘤与肾脏的比值从2小时的1.25到注射后192小时的22.29不等,这将有利于RayzeBio后续的剂量爬坡,如果使用23 Gy作为肾脏的剂量限制时,最大肿瘤剂量估计约高达209 Gy。总之,临床前数据支持RAYZ-8009作为肝癌患者治疗核药的临床研究。
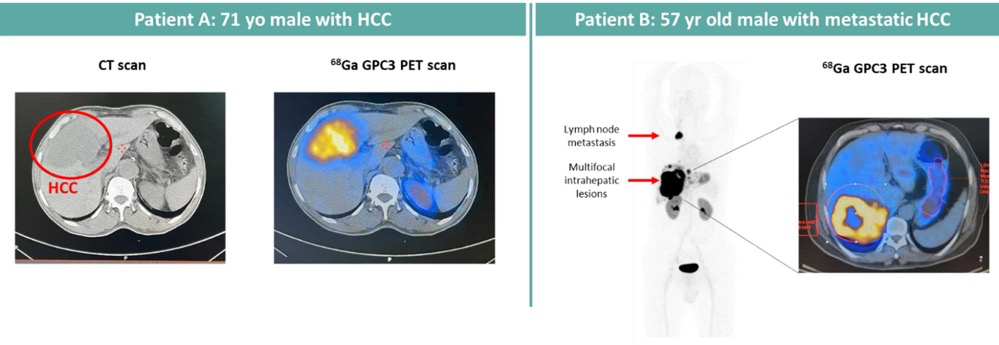
源自RayzeBio官网展示的基于患者的数据
2024年6月起,临床研究结果陆续披露。在去年SNMMI会议投稿的摘要信息显示:研究扫描了 15 名患者(5 名动态患者;10 名静态患者),一名疑似患有 HCC 的患者在随访期间并未出现 HCC。另一名患者同时患有转移性前列腺腺癌,但在定性和定量方面均未显示摄取(SUV 值小于 1.0),经免疫组化证实,同一患者(患有前列腺癌)的三个 HCC 病灶被认为是 GPC3 阴性;PET/CT 上的 HCC 病灶内 GPC3 表达不均,说明了疾病的异质性。在定性评估中,大多数已知、疑似或不确定的 HCC 病灶都显示出摄取。总共有 38 个 HCC 病变在不同的时间点进行了成像,包括上述 GPC3 阴性病变。在 60 分钟时,平均 SUVmax 为 20.0(范围为 2.7 - 95.3),平均 SUVmean 为 10.2(范围为 1.0 - 49.2)。随着时间的推移,健康肝脏和血池的摄取量迅速下降,在用药 45 分钟后变得较低(SUVmean <1.6),并呈持续下降趋势,直至用药 4 小时后(平均 SUVmean = 1.0)。而 HCC 和 TLR 的情况恰恰相反,它们在用药后 4 小时内持续上升(注射后 18 分钟、1 小时和 4 小时的平均 TLR 分别为 5.5、8.9 和 19.2)。在单个病灶分析中,TLR 在注射后 60 - 120 分钟之间最高。胃壁的摄取量在第一小时内逐渐增加,之后逐渐减少(注射后18分钟、1小时和4小时的平均SUVmean分别从18.9到22.6,再回到14.9)。
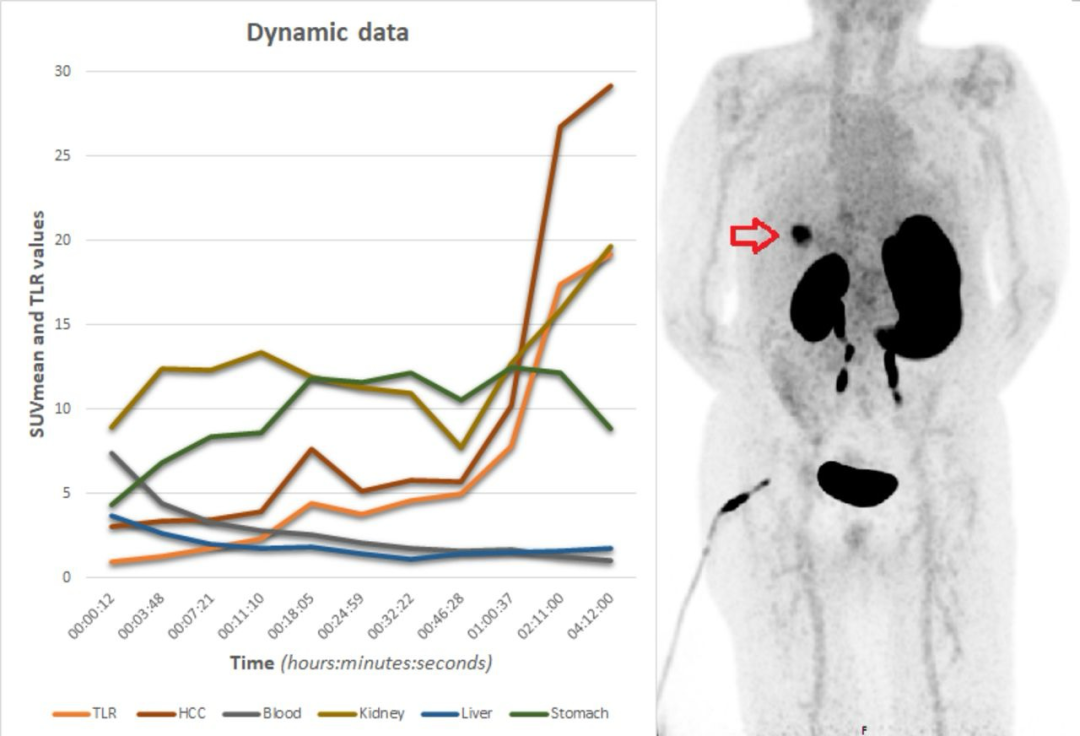
Journal of Nuclear Medicine June 2024, 65 (supplement 2) 241739
2024年9月,临床研究结果发表在核医学期刊JNM上。研究共对24名患者(5名接受动态方案,19名接受静态方案)进行了扫描,未发生不良事件。2名患者未检测到病灶,且在随访中未发现HCC。共检测并分析了50个病灶。这些病灶的平均SUVmax为19.6(范围2.7-95.3),平均SUVmean为10.1(范围1.0-49.2),在给药后约60分钟时测量。非肿瘤肝脏和血池的摄取在给药后迅速下降,45分钟后变得可以忽略不计(平均SUVmean < 1.6),并且在给药后4小时持续下降(平均SUVmean为1.0)。相反,HCC病灶的SUV和TLR在给药后4小时内持续增加。在单个病灶分析中,TLR在给药后60至120分钟之间达到最高值。胃底的摄取在给药后45分钟内逐渐增加(SUVmax达到31.3),随后逐渐下降。研究证实了[68Ga]Ga-RAYZ-8009安全且能够实现GPC3阳性HCC的高对比度成像,且在大多数正常器官中快速清除,在HCC的诊断和分期方面具有潜力,值得进一步研究。
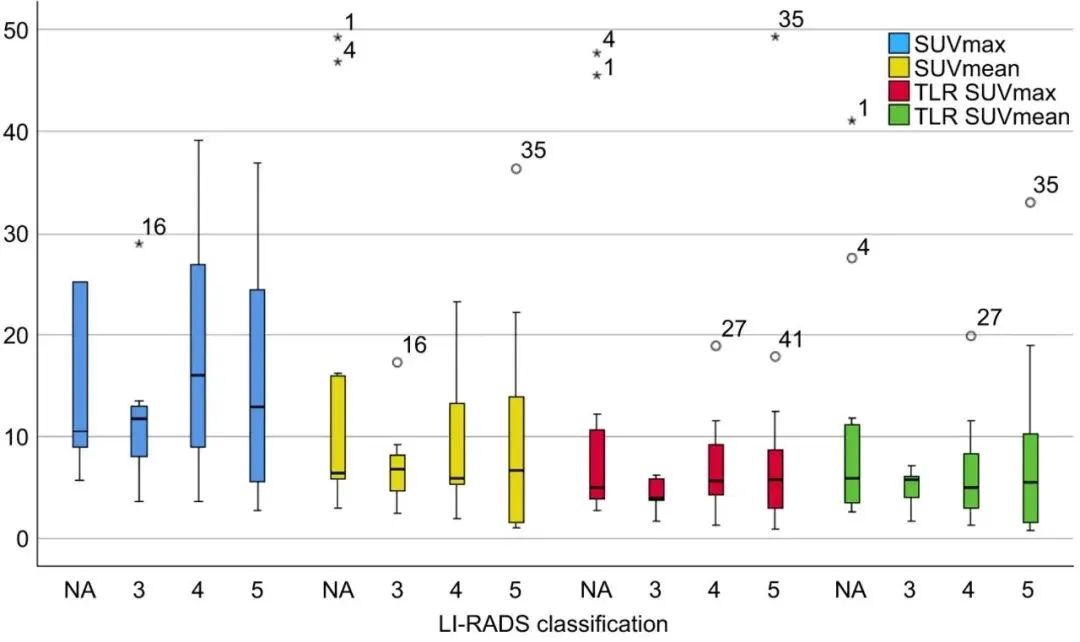
Journal of Nuclear Medicine September 2024, jnumed.124.268147
该药物的研发历程始于2022年12月6日首次披露,随后在2023年6月1日完成首个转化医学研究。关键的临床开发阶段于2024年12月10日正式启动,通过登记I/1b期单臂开放标签试验(NCT06726161),评估225Ac-RAYZ-8009与68Ga-RYZ-GPC3这对诊疗一体化组合在肝细胞癌中的应用。研发方RayzeBio, Inc.于2024年12月12日获得首个化合物/序列专利。当前全球最高研发阶段为I期临床(Active状态),研究周期为2023年6月1日至2031年1月1日,主要在美国开展。小编将持续关注并及时更新最新研究进展,实时报道。

切入前列腺癌市场,避开PSMA红海竞争
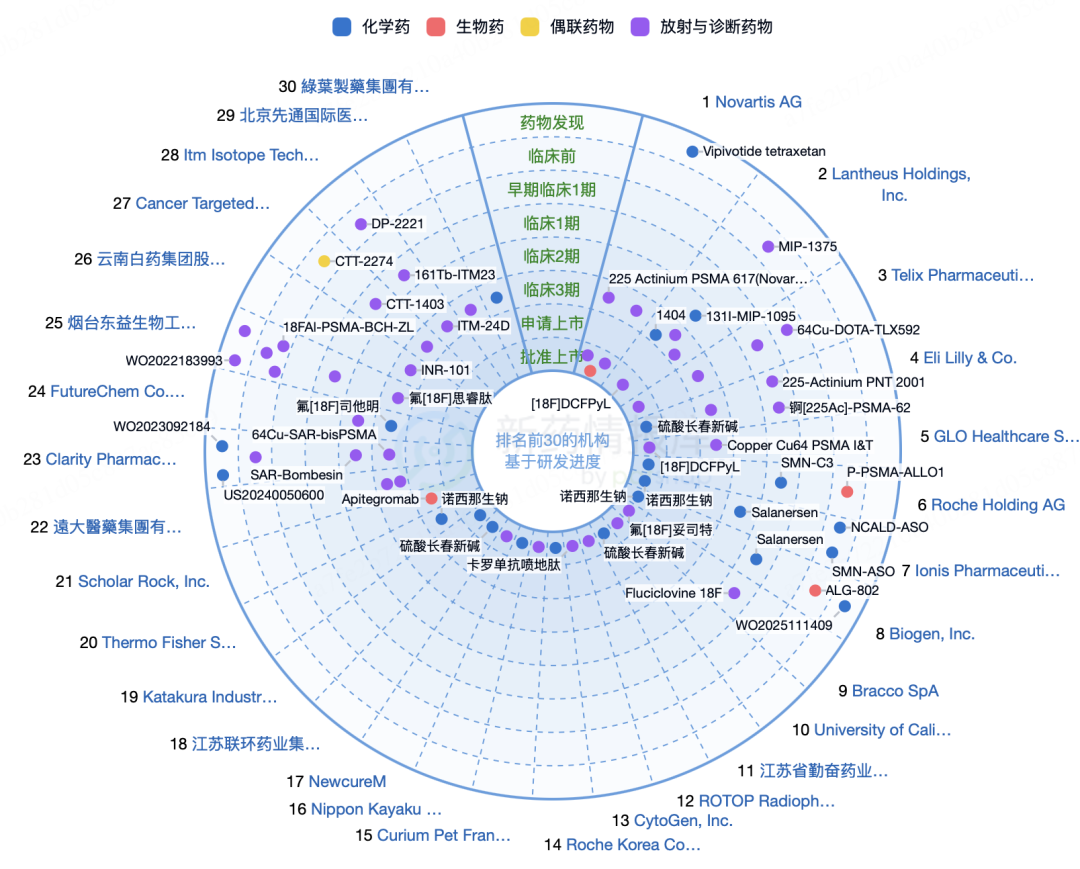
PSMA靶点的核药研发状态(数据更新截至时间为2025.06.12)
在前列腺癌治疗领域,诺华的PSMA617虽已成为放射性配体疗法的标杆产品,但靶点内卷竞品诸多,赛道拥挤。BMS旗下RayzeBio却另辟蹊径,通过战略性收购OncoACP3布局差异化赛道——以13.5亿美元(含3.5亿首付及10亿里程碑)获得靶向酸性磷酸酶3(ACP3)的全球权益,该新兴靶点不仅在前列腺癌中呈现特异性高表达(健康组织几乎不表达),更与PSMA靶点无交叉耐药性,其独特的生物学特性使其具备成为Best-in-Class药物的潜力,有望在竞争激烈的PSMA红海市场之外开辟新的治疗蓝海。
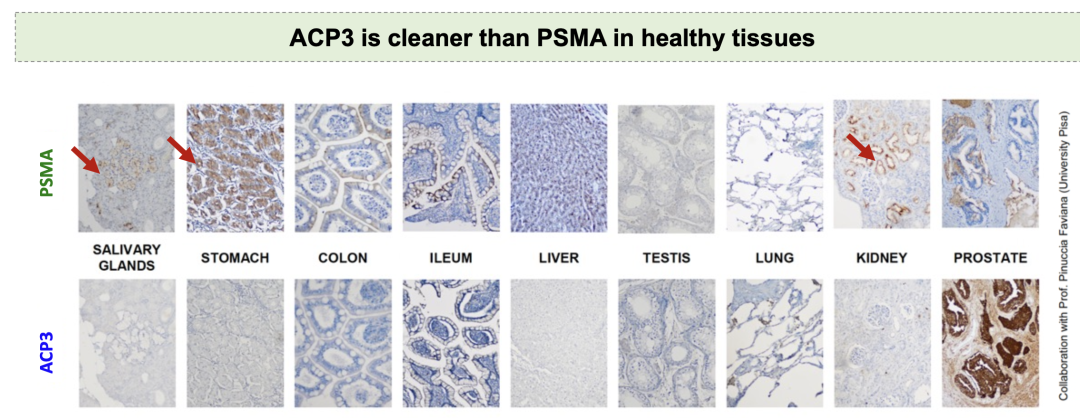
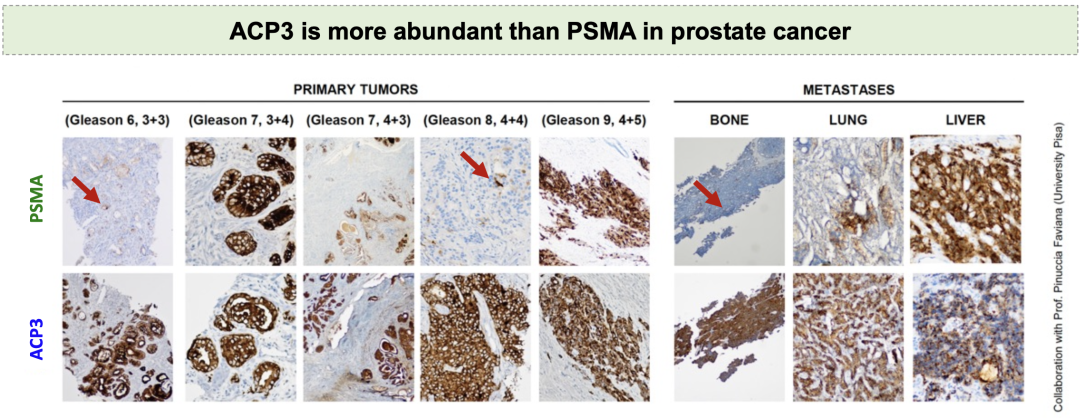
酸性磷酸酶3(ACP3)在癌性前列腺组织中高度表达,而在绝大多数正常器官(包括健康前列腺)中几乎无法检测,展现出比当前主流靶点PSMA更强的肿瘤特异性。PSMA虽然在唾液腺、胃肠道和肾脏等正常组织中也有表达,但其表达水平通常比前列腺癌细胞低100-1000倍,且多位于非直接接触血液循环的部位。相比之下,ACP3具有更低的非靶组织摄取和更高的肿瘤表达量,在“干净性”与“靶向效率”两方面均显著优于PSMA,使其成为前列腺癌诊疗中更具潜力的新型靶点。
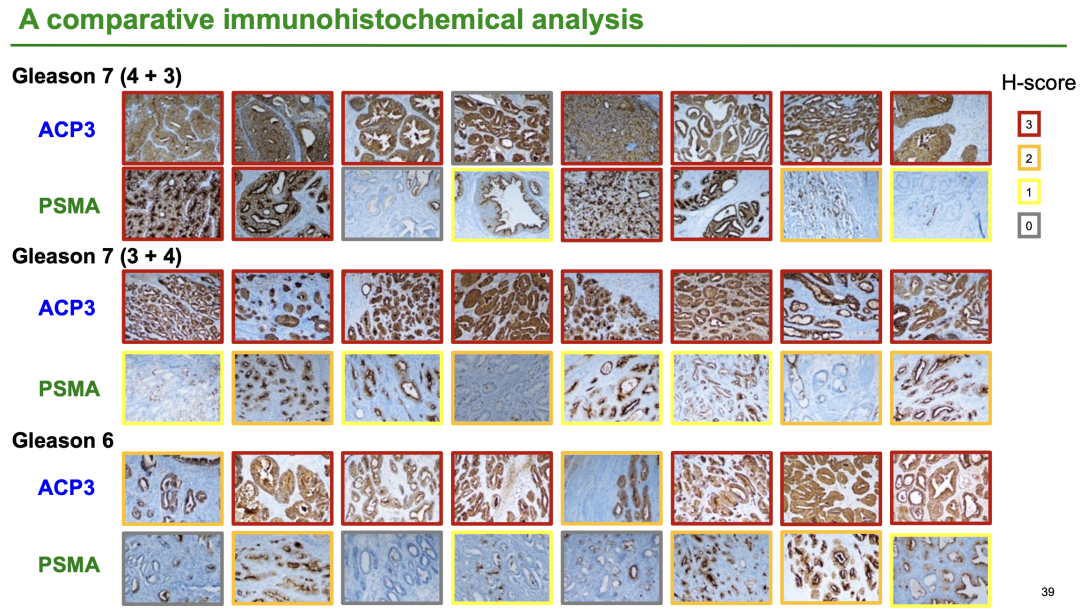
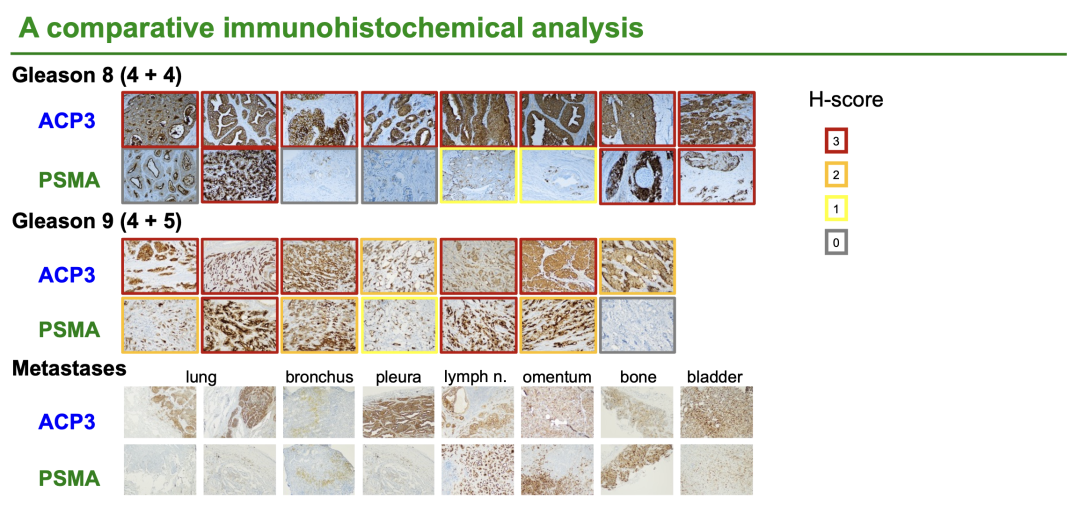
Philochem最新研究采用免疫组化技术(IHC)对39例前列腺癌患者的连续组织切片进行系统分析,通过同步检测PSMA与ACP3的表达特征,发现两者在不同Gleason评分肿瘤中存在显著差异。研究显示:87%(34/39)的样本呈现ACP3强阳性表达(H-score=3),而PSMA的强阳性率仅为23%(9/39)。这一发现表明,相较于PSMA,ACP3在前列腺癌组织中可能具有更广泛且稳定的表达特征,提示其作为前列腺癌诊断或治疗靶点的潜在生物标志物价值值得进一步研究。
目前,针对酸性磷酸酶3(ACP3)靶点的前列腺癌治疗和诊断产品尚未有获批上市的药物,但有多款处于临床研究阶段的候选药物。
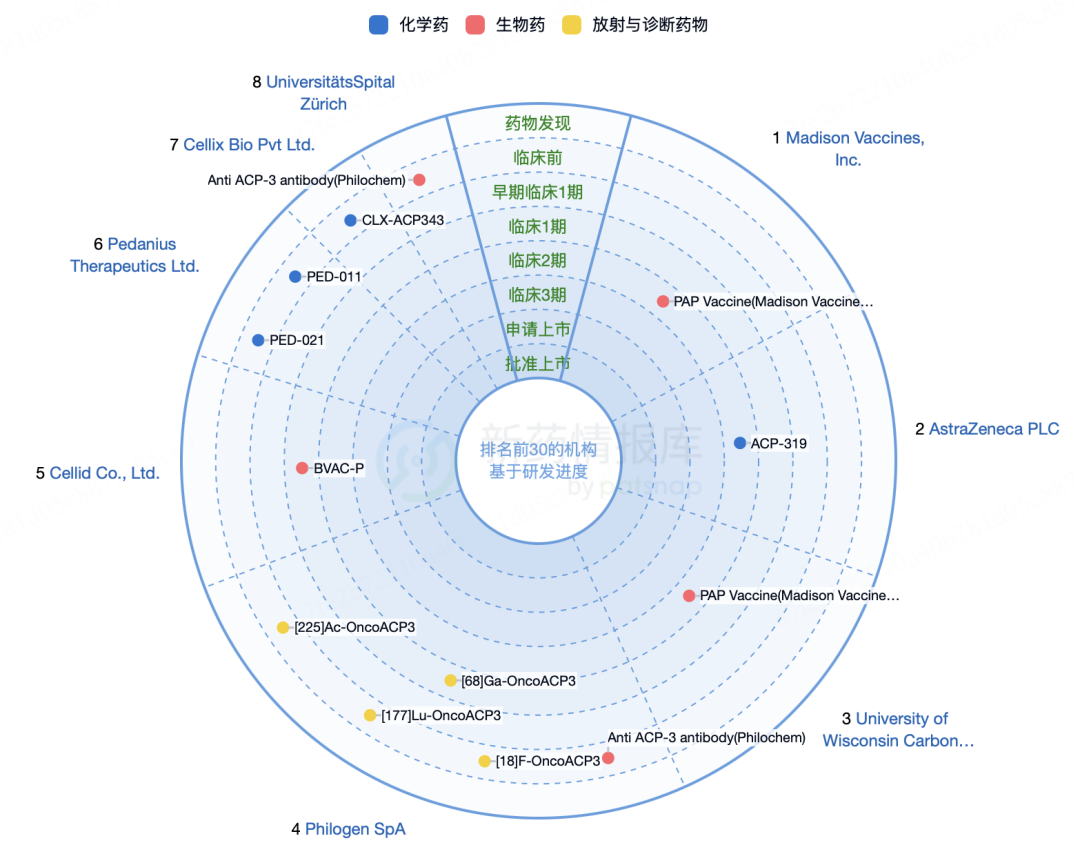
ACP3靶点的核药研发状态(数据更新截至时间为2025.06.12)
当前前列腺癌放射性药物(RDC)领域的主流靶点PSMA已形成激烈竞争格局,诺华的Pluvicto(177Lu-PSMA-617)作为首个获批的PSMA靶向疗法,2024年销售额达13.92亿美元。除诺华外,礼来、拜耳等企业均在布局PSMA靶点(如177Lu-PNT2002、225Ac-J591),同质化竞争仍在持续加剧。相比之下,ACP3(酸性磷酸酶3)靶点的开发仍处于早期阶段,目前仅有Philochem/BMS开发的OncoACP3进入临床阶段,无其他公开竞品,相比177Lu-PSMA靶向药物(如诺华Pluvicto),OncoACP3凭借更干净的靶向性和α核素(225Ac)的精准杀伤力,可能成为耐药或不耐受PSMA疗法患者的新选择,展现出成为Best-in-Class核药的潜力,有望填补差异化市场空白。
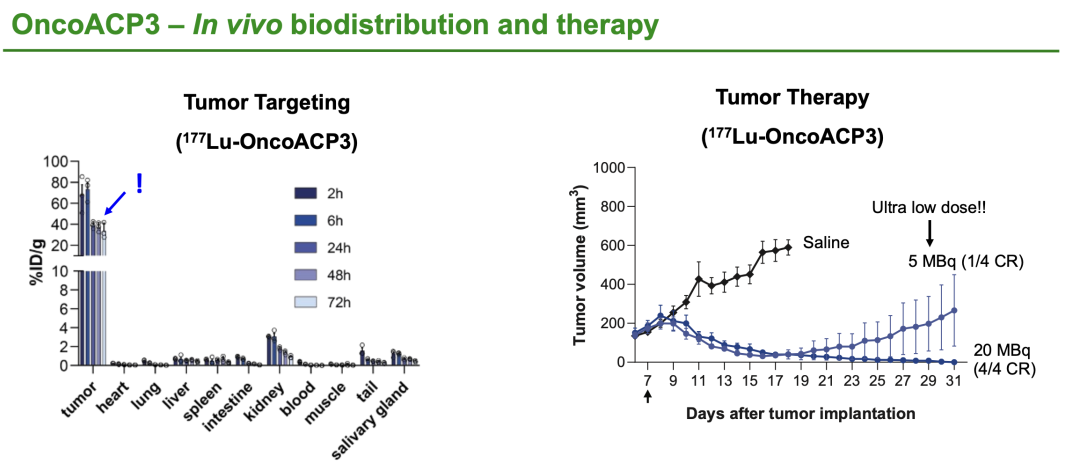
临床前数据展示
目前Philogen集团旗下瑞士子公司Philochem AG已完成化合物的筛选、专利申请与布局、并在临床前的研究中证实了新核药的安全性与有效性:如上图所示,OncoACP3在荷瘤小鼠模型中显示出极低的非靶器官摄取(如肾脏、唾液腺),而177Lu-OncoACP3在低剂量(5–20 MBq/小鼠)下即表现出显著抗肿瘤活性,且未观察到传统PSMA靶向疗法的毒性问题。

Philochem Website
2025年6月10日,Philochem AG与百时美施贵宝(BMS)全资子公司RayzeBio正式达成一项价值高达13.5亿美元的全球授权协议。根据协议条款,Philochem将获得3.5亿美元预付款及最高10亿美元的里程碑付款,外加全球净销售额的中个位数至低双位数(5%~12%)特许权使用费。

该交易授权RayzeBio独家开发、生产和商业化靶向前列腺癌新靶点ACP3的放射性药物OncoACP3:诊断核药(68Ga-OncoACP3)目前处于I期试验(NCT06840535),旨在评估其在前列腺癌患者中的安全性、剂量学和生物分布特性。该试验于2025年2月在意大利3个研究中心启动,计划招募20例患者,预计同年12月完成入组。初步数据已显示优异的肿瘤选择性和诊断潜力;治疗核药(225Ac-OncoACP3)目前IND-enabling进行中,计划推进至治疗性I期临床。交易预计将于2025年第三季度完成,需满足常规成交条件及监管批准。
差异化布局,引领行业创新
在肝癌治疗领域,RayzeBio押注GPC3这一高度特异性的靶点(在75%肝细胞癌中高表达而正常组织几乎不表达),通过诊疗一体化平台(RYZ801/RYZ811)实现了从诊断到治疗的闭环管理。此次APC3靶点的收购则是BMS通过RayzeBio布局前列腺癌放射性药物领域的关键举措,旨在填补其管线中与PSMA靶点差异化的创新疗法空白。公司选择避开PSMA红海市场,以13.5亿美元收购ACP3靶点药物全球权益,该靶点不仅与PSMA无交叉耐药,更展现出成为best-in-class药物的潜力。若未来临床数据持续积极,OncoACP3有望凭借ACP3靶点的高特异性和“诊疗一体化”设计,成为前列腺癌领域的Best-in-Class核药,尤其为PSMA疗法不耐受或耐药患者提供新选择。
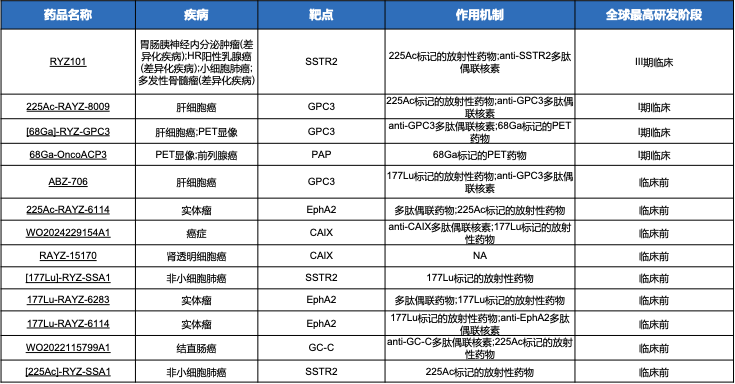
现有管线梳理,(数据更新截至时间为2025.06.12)
RayzeBio的成功印证了核药领域的竞争已从“跟随式创新”转向“靶点+核素+临床”的系统性突破。聚焦未满足的临床需求,选择肝癌(GPC3)和前列腺癌(ACP3)等缺乏有效疗法的适应症,避免与PSMA赛道的同质化竞争;打造技术差异化标签,通过α核素布局和头部药物筛选企业达成合作提升技术壁垒;借助MNC的并购资源,快速推进从临床前到商业化的全链条布局。
由此可见,核药唯有“真创新”(敢于尝试First-in-Class靶点)与“硬数据”(临床价值量化)的结合,方能有望赢得资本与市场的双重认可。