2026-01-23
[225Ac]Ac核素与ACTION-1研究简介
α放射性治疗药物采用发射α粒子的放射性核素,例如镭[223Ra]、锕[225Ac]、钍[227Th]、砹[211At]、铅[212Pb]、铋[213Bi]等。α粒子具有传能线密度(Linear Energy Transfer,LET)高、电离辐射效应大、细胞杀伤效率高和射程短的特点,通常在组织中穿透距离约40-100μm(<10个细胞直径)。α粒子的高LET可使肿瘤细胞核中的DNA双螺旋链断裂而引起细胞凋亡,并且所需放射性剂量较低,数个穿过细胞核的α粒子足以杀死细胞。
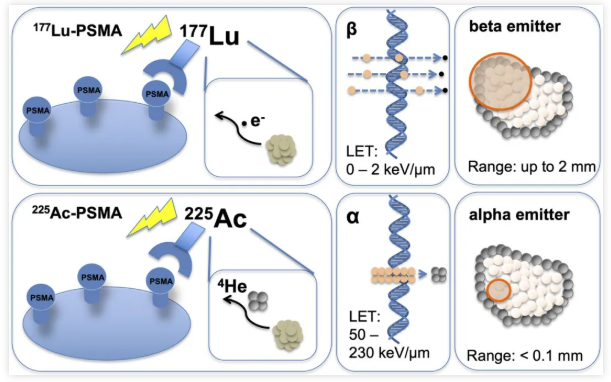
225Ac-PSMA与177Lu-PSMA放射生物学效应比较
225Ac(锕-225),具有9.92天的半衰期,在临床前和临床研究中展现出了显著的疗效,这主要归因于其衰变过程中释放的四个α粒子。尽管如此,225Ac本身并不发射可直接用于成像的γ射线,因此其分布和成像通常需依赖于其衰变链中的子核放射性核素221Fr(半衰期为4.80分钟;218 keV;11.4%)和213Bi(半衰期为45.6分钟;440 keV;25.9%)所释放的γ射线。221Fr和213Bi的探测是在连续的α衰变之后进行的,这一过程可能会因为子核反冲和放射性药物共轭形式的分解而带来一定的不准确性。因此,能够直接且定量地在体内检测锕系元素对于优化临床前放射性药物的开发和临床治疗计划至关重要。
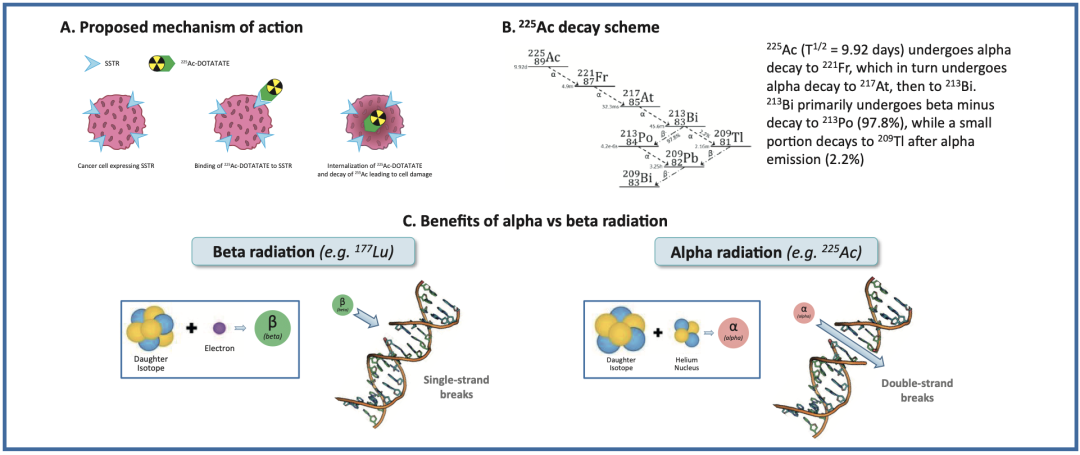
用于放射性核素治疗的放射性核素RYZ101(225Ac-DOTATATE)
RYZ101(225Ac-DOTATATE)是一种α粒子放射药物治疗药物,正在开发用于治疗表达生长抑素受体2(SSTR2+)的实体瘤。ACTION-1(NCT05477576)是一项两阶段的全球性、随机、对照、开放标签的1b/3期试验,比较RYZ101治疗与标准治疗在不可手术、晚期、SSTR2+、分化良好的胃-肠-胰腺神经内分泌肿瘤(GEP-NETs)患者中的疗效,这些患者的病情在先前的177Lu标记的生长抑素类似物治疗后有所进展。在ACTION-1试验的1b期部分,首次开展了剂量测定子研究,旨在评估获取225Ac成像数据以估算RYZ101对关键器官(主要目标)和肿瘤(次要目标)吸收剂量的可行性,该研究成果已于2023年6月在JNM的会议报告中公布,确认了利用225Ac进行成像以及获取剂量测定所需定量信息的可行性。
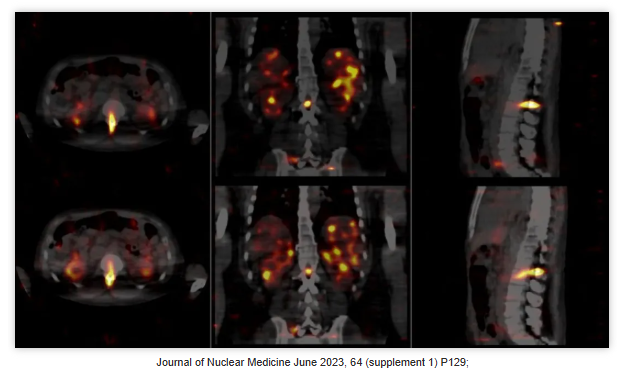
在ACTION-1试验的1b期部分,主要目标是确定RYZ101的推荐3期剂量。为确保至少有五名可评估的患者,有八名患者参与剂量测定子研究。使用SPECT/CT图像对第1周期和第4周期进行剂量测定计算,分别在注射后4 ± 1小时、24 ± 2小时和168 ± 24小时进行。在进行225Ac标记的SPECT/CT扫描时,均采用了高能准直器,并配备了相应的均匀性校正图谱。数据采集是在三个特定的能量窗口(92keV、218keV和440keV,窗口宽度分别为25%、20%和20%)下进行的。通过运用双放射性核素定量SPECT重建技术,获得了221Fr和213Bi的分布图像,并对此过程中可能出现的串扰及其他物理因素导致的图像结果进行了补偿。对肝脏、肾脏、脾脏、红骨髓(第三至第五腰椎)以及选定肿瘤的放射性活度进行了精确的定量分析。利用医学内辐射剂量(MIRD)委员会推荐的S值方法,并结合Rapid软件包中的3D-RD-S工具,计算了目标器官和病变的吸收剂量。总体来看,研究首次揭示了213Bi主要与靶向载体(DOTATATE)共存,仅有少量进入肾脏;ACTION-1剂量测定数据的初步结果支持RYZ101在治疗SSTR+ GEP-NETs时具有较好的肿瘤与背景比,10.2 MBq的固定剂量已被确定为推荐用于3期临床试验的剂量。
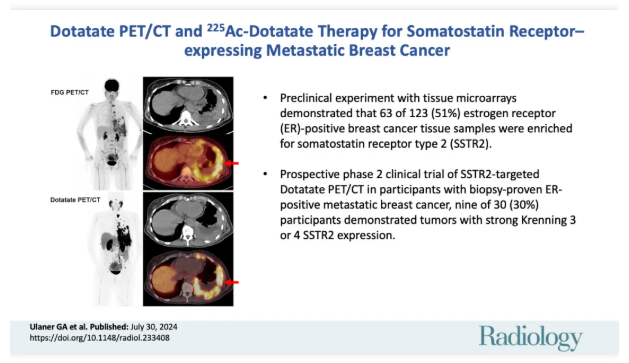
核药剂量测量的目的在于估算正常组织和肿瘤的吸收剂量,进而预测辐射的生物效应。在对α放射性药物进行剂量测定时,虽然可以将α粒子的估计吸收剂量乘以相对生物学效应(RBE)值,但还需考虑放射性核素的微观分布差异对预测毒性与实际观察到的毒性的影响。鉴于目前技术尚无法精确测量人体给药后α粒子放射性药物及其衰变子体的活度,因此在能够准确定量的技术出现之前,可以采用替代方法来评估肿瘤和正常器官的辐射暴露。这些方法可以根据剂量-反应关系、临床有效性及安全性数据来指导剂量选择的优化。对于无法直接显像的α粒子放射性治疗药物,建议使用已建立的影像技术来检测放射性核素标记的靶向部分。例如,可以使用SPECT可检测的单光子发射放射性核素(如铟[111In]或锝[99mTc]),或PET可检测的正电子发射放射性核素(如锆[89Zr]、镓[68Ga]、铜[64Cu]、氟[18F])。由于不同核素的标记物在能量分布、吸收剂量率和药代动力学等方面可能存在差异,这些替代方法仅能作为评估肿瘤和正常器官α粒子辐射暴露的辅助手段,实际的α放射性药物分布情况仍需通过进一步的体内研究来确定。由于患者的基础疾病和个体差异,辐射剂量学具有高度的变异性,这限制了其在预测个体毒性和/或有效性方面的能力。因此,辐射剂量学应作为剂量递增研究中评估临床安全性和有效性的辅助信息。在临床研究中,剂量递增和个体患者管理的决策应基于临床安全性评价,而非仅仅依赖于计划的辐射吸收剂量限值。
[225Ac]Ac核素替代显像剂:[226Ac]Ac
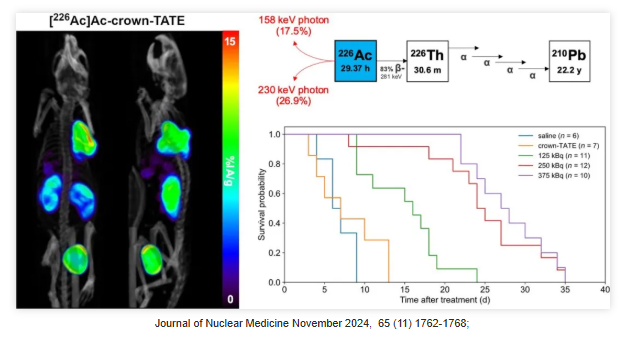
225Ac作为一种具有治疗潜力的放射性同位素,因其衰变链中释放的α粒子而受到关注,但其缺乏直接可成像的γ辐射限制了对其体内分布的直接观察。因此使用替代显像剂如226Ac对于评估225Ac的体内分布、优化治疗计划、监测疗效以及确保治疗的安全性和个体化至关重要。226Ac(半衰期为29.37小时)非常适合作为与225Ac放射性药物匹配的治疗对,因为它们具有相同的体内放射化学和药代动力学特性。226Ac通过其158和230 keV的γ辐射可以被SPECT成像,并且由于其子代226Th的α衰变,也可以被认为是一种独立的治疗同位素。226Ac通过β衰变转化为226Th,后者通过非常短半衰期的子核发射4个高能α粒子,累积能量为27.7MeV。近日一项发表在《核医学杂志》(Journal of Nuclear Medicine [JNM])期刊的研究评估了226Ac(半衰期29.37小时)作为一种独立的治疗同位素的可行性,并展示其作为治疗放射性核素的潜力。
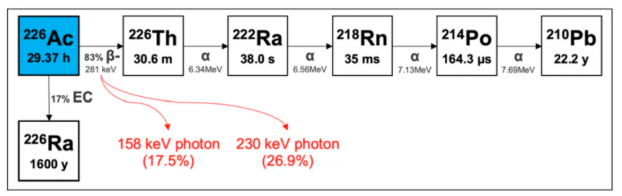
226Ac衰变链及其物理性质
研究结果揭示了[226Ac]Ac-crown-TATE在体内的定量SPECT成像与体外测量结果高度一致,显示出在肿瘤中的高摄取率(注射后5小时内超过30%IA/g)及持久滞留,平均吸收剂量为222 mGy/kBq。[226Ac]Ac-crown-TATE的治疗显著抑制了肿瘤生长并延长小鼠生存期,且在整个研究过程中未观察到体重下降或毒性反应。总体而言,该研究凸显了226Ac作为一种独立的治疗性同位素在诊断和治疗方面的潜力。它不仅证实了在匹配225Ac放射性药物中用于剂量测定的诊断能力,而且未来的研究将进一步探讨最大剂量和毒性问题,以深入挖掘226Ac放射性药物的治疗潜力。此类替代显像剂能够提供关键的剂量学信息,助力研究者和临床医生更深入地理解225Ac的生物分布特性,从而在靶向α治疗中实现对肿瘤的更精确杀伤,同时最大限度地减少对周围正常组织的损害。此外,替代显像剂的应用对于新药开发和治疗对的建立也具有重要意义,它将进一步推动核医学领域的发展,为患者带来更有效和更安全的治疗选择。
[225Ac]Ac核素替代显像剂:[134Ce]Ce
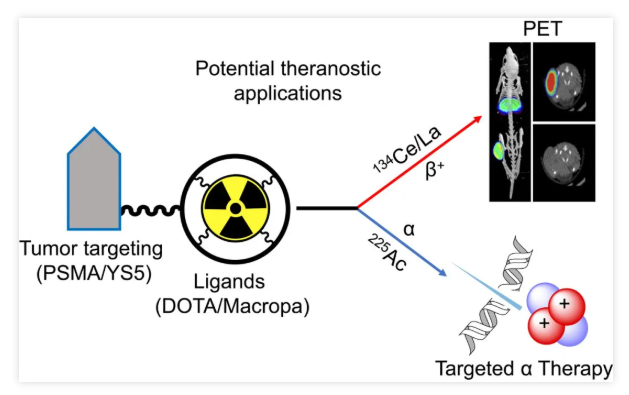
2023年7月,一项发表在《核医学杂志》(Journal of Nuclear Medicine [JNM])期刊的研究详细评估了铈-134(134Ce)与镧-134(134La)作为正电子发射断层扫描(PET)成像治疗诊断对,用于锕-225(225Ac)α放射性治疗的潜力。研究通过使用DOTA和MACROPA螯合剂,实现了134Ce的高效放射性标记,并将其应用于前列腺癌成像剂PSMA-617和MACROPA-PEG4-YS5的体内药代动力学特性评估,与相应的225Ac类似物进行了比较。该研究结果表明,134Ce与225Ac的化学性质和药代动力学特性相似,134Ce/134La对可能作为PET成像替代品用于基于225Ac的放射配体治疗,其中134Ce-MACROPA.NH2和134Ce-DOTA在体内显示出高稳定性,且其生物分布与相应的225Ac复合物相似,而134Ce-PSMA-617和134Ce-MACROPA-PEG4-YS5在前列腺癌模型中的PET成像和生物分布结果也支持了134Ce/134La对作为225Ac的成像替代品的潜力。
2024年6月,另一项发表在《European Journal of Nuclear Medicine and Molecular Imaging》期刊的研究进一步对225Ac(锕-225)和134Ce(铈-134)标记的示踪剂进行了直接比较,评估了其作为匹配治疗诊断对的潜力。研究选取快内化和慢内化的模型,评价了它们的体内相似性、子核再分布和临床转化潜力。PSMA-617前体和macropa 基mcp-PEG8-Tz 分别用225Ac和134Ce进行放射性标记,并在体外和体内通过标准(放射)化学方法进行比较。
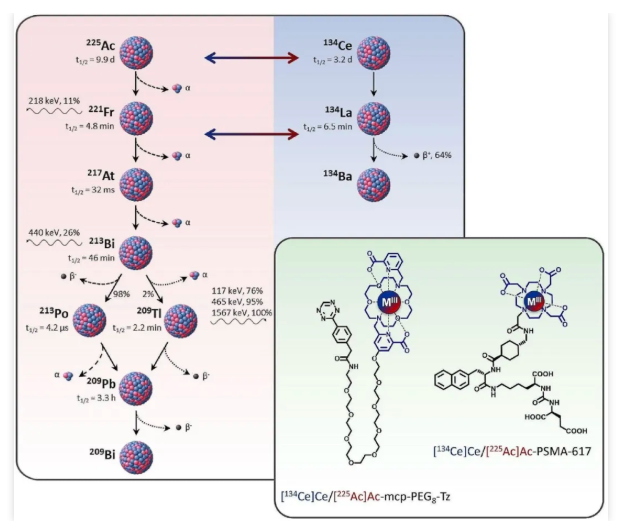
体内外研究结果表明,225Ac与134Ce标记的示踪剂展现出相似的药代动力学特性,从而验证了它们作为匹配治疗诊断对的潜力。然而,对于134Ce标记的前体进行的PET成像分析显示,其定量准确性极大地依赖于示踪剂的内化效率,这一现象归因于134Ce衰变产生的子核134La在体内的再分布特性。基于此,如PSMA-617等快速内化载体的放射性示踪剂与134Ce/134La治疗诊断对相匹配,而那些内化速度慢的225Ac标记示踪剂则难以通过134Ce PET成像获得准确的定量数据。在采用慢内化载体的情况下,134Ce可能不足以作为225Ac的理想配对,因为134La的体内再分布可能导致对肿瘤摄取量的低估。尽管如此,这一特性为非侵入性监测225Ac子代的再分布提供了可能,这在未来的研究中将有助于深入探究示踪剂的内化过程、受体的转运机制以及肿瘤微环境的变化。因此,结合快速内化放射性示踪剂与较晚的成像时间点(例如24小时后)是优化该治疗诊断对策略的关键。
结语
锕-225(225Ac)作为一种具有巨大潜力的α粒子发射核素,在肿瘤靶向放射性核素治疗领域因其卓越的能量传递效率、适宜的半衰期、短程粒子射程以及出色的配位特性而备受关注,为多种肿瘤治疗提供了创新的治疗途径。尽管如此,225Ac的临床应用仍面临多重挑战,包括核素供应的限制、高效的标记技术与适配螯合剂的筛选、提升治疗的靶向精准性,以及如何减轻对周围正常组织的辐射损伤。尽管存在挑战,但随着剂量学方法、前体设计和放射性药物递送技术的不断创新,α粒子核素治疗有望发展成为高效的治疗手段,显著提高肿瘤治疗的效果和安全性。